我院朱志教授课题组与合作者发展了膜结合型胞内E3泛素连接酶嵌合体靶向降解膜蛋白的新方法,相关成果以“Membrane-Bounded Intracellular E3 Ubiquitin Ligase-Targeting Chimeras (MembTACs) for Targeted Membrane Protein Degradation”为题近日在线发表于Angew. Chem. Int. Ed. (DOI: org/10.1002/anie.202501857)。
细胞膜蛋白在人类多种生理和病理过程中发挥关键作用,其过度激活或突变可导致癌症等疾病。靶向蛋白降解(TPD)是一种通过降解疾病相关靶蛋白实现治疗的有效策略,有望克服传统抑制剂的局限性,挑战“难成药”靶点,为药物开发提供新的靶向治疗手段。在TPD策略中,蛋白水解靶向嵌合体(PROTAC)技术通过泛素-蛋白酶体系统特异性降解疾病相关靶蛋白,是研究最为成熟的系统,已成为目前新药研发领域火热的技术之一。然而,传统PROTAC利用胞内E3泛素连接酶,只能降解胞内蛋白,且因嵌合体分子量大导致水溶性和细胞渗透性差。少数报道的依赖细胞表面E3泛素连接酶降解膜蛋白的工作,存在酶的种类有限且表达不稳定、基于抗体的嵌合体设计复杂繁琐的问题。因此,亟需开发新型、易合成且适应性更强的蛋白降解剂,以实现细胞膜蛋白的特异性泛素化降解。
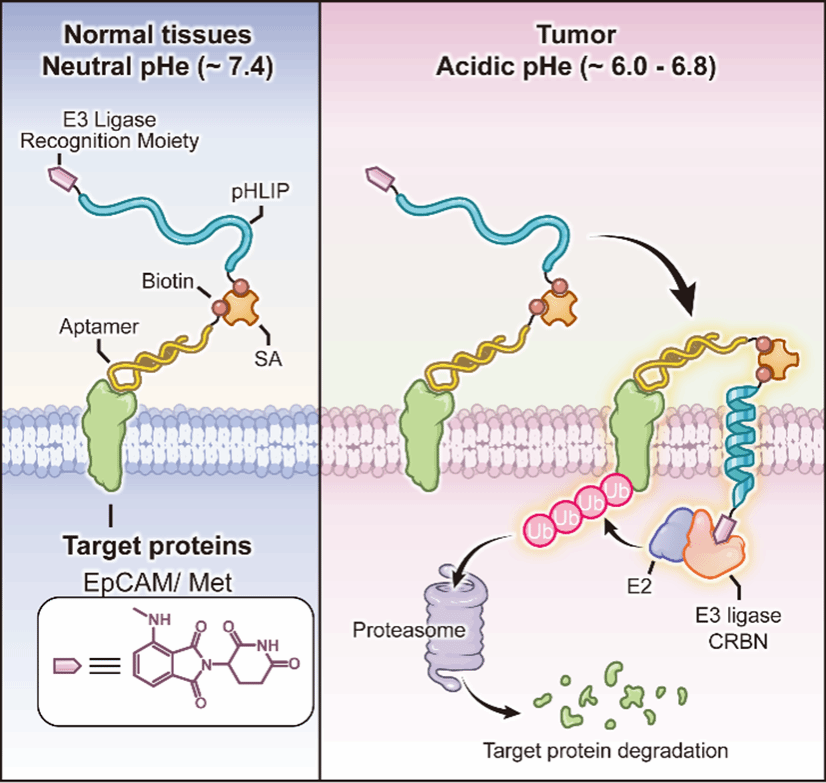
为解决上述问题,团队提出了一种利用细胞内E3泛素连接酶降解膜蛋白的新型PROTAC方法,命名为膜结合型胞内E3泛素连接酶靶向嵌合体(MembTACs)。MembTACs包含三个部分(如图):pH敏感肽段(pHLIP)仅在肿瘤微酸环境下插入细胞膜,在正常组织中保持惰性,减少副作用;pHLIP插入细胞膜内的C端为降解模块,连接小分子药物泊马度胺,将细胞内E3泛素连接酶CRBN招募至膜内侧;pHLIP的N端为识别模块,可灵活替换核酸适体或抗体,识别细胞膜蛋白。从而利用CRBN泛素化特定膜蛋白的胞内结构域实现降解。MembTACs无需细胞跨膜递送过程即可有效利用细胞内E3泛素连接酶实现肿瘤细胞膜蛋白的降解。这一策略不仅提高了降解效率,更将传统PROTAC的应用范围扩展至膜蛋白领域,有望为靶向蛋白降解技术和临床药物设计开辟新思路与应用前景。
该工作在我院朱志教授和浙江省肿瘤医院赏金标主任的共同指导下完成,我院2021级博士生莫蒙武为论文的第一作者。研究工作得到国家重点研发计划(2021YFA0909400)、国家自然科学基金(22325404、21974113、21927806)和中央高校基本科研业务费(20720210001、20720220005)等项目资助。
论文链接:https://onlinelibrary.wiley.com/doi/10.1002/anie.202501857
